Module 2 Inbrengen
Uitgangsvraag
Welke maatregelen dienen genomen te worden bij het inbrengen van een transurethrale katheter om het risico op een urineweginfectie te verminderen?
Aanbevelingen
- Breng een transurethrale katheter schoon in. Dit houdt in: er wordt gebruik gemaakt van een onderlegger, er worden niet-steriele handschoenen gedragen en de genitaliën worden gereinigd met leidingwater. Algemene voorzorgsmaatregelen dienen altijd toegepast te worden.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor deze module is een systematische literatuuranalyse uitgevoerd naar het effect van schoon (in plaats van steriel) inbrengen van een transurethrale katheter op de uitkomstmaten urineweginfectie en bacteriurie. Eén studie beschreef de volledige vergelijking van schoon versus steriel inbrengen van een transurethrale katheter voor de uitkomstmaat urineweginfecties. De risk ratio was 0.89 (95% CI: 0.62, 1.29). Vanwege beperkingen in de studieopzet en imprecisie is de kwaliteit van het bewijs zeer laag. Twee studies (waarvan een uit de systematische review van Mitchell 2021) vergeleken verschillende middelen voor het reinigen van de genitaliën. Vanwege beperkingen in onder andere de studieopzet en inconsistentie is de kwaliteit van het bewijs zeer laag. Voor de uitkomstmaat bacteriurie werden geen studies gevonden die het schoon inbrengen van een katheter vergeleken met steriel inbrengen. Vijf studies vergeleken verschillende middelen voor het reinigen van de genitaliën. Het gepoolde effect was 1.24 (95% CI: 0.93 – 1.66). Het reinigen van de genitaliën met antiseptica lijkt geen effect te hebben op het ontstaan van bacteriurie in vergelijking met het reinigen met (leiding)water. De kwaliteit van het bewijs was laag.
Het schoon inbrengen van een transurethrale katheter omvat het gebruik van niet-steriele handschoenen, een schoon werkveld en het reinigen van de genitaliën met (leiding)water. Het steriel inbrengen omvat het gebruik van steriele handschoenen, het creëren van een steriel werkveld en het reinigen van de genitaliën met steriel water of een desinfectans.
De geïncludeerde studies in deze literatuur samenvatting beschreven alleen het middel voor het reinigen van de genitaliën voor het inbrengen van de katheter, behalve de studie van Duffy (1995) die daadwerkelijk de vergelijking tussen schoon en steriel inbrengen van een katheter maakte. In de overige studies werd niet beschreven in hoeverre of naast het gebruikte reinigingsmiddel de katheter op een schone of steriele wijze werd ingebracht.
Het steriel inbrengen van een katheter is een handeling die veelal met twee personen gedaan wordt. Steriel werken kan een gevoel van schijnveiligheid creëren en afleiden van de aandacht voor basismaatregelen, zoals het toepassen van een goede handhygiëne. Ook kunnen desinfectans zoals chloorhexidine irritatie geven bij het toepassen op een niet-intacte huid. Zelfs voor werken in een omgeving die verontreinigd is (bijvoorbeeld met feces) is geen evidence gevonden die de meerwaarde van gebruik van desinfectans kan ondersteunen. Reinigen met (steriel) water en het toepassen van basismaatregelen op het gebied van hand- en omgevingshygiëne hebben ook hier de voorkeur.
Kortom: steriel werken vraagt een grotere belasting qua tijd, middelen en personele inzet, en heeft geen meerwaarde in het voorkómen van (katheter gerelateerde) urineweginfecties.
Pathofysiologische overwegingen
Zoals beschreven in module 1 Indicaties is de blaas geen steriele omgeving en wordt ook de urethra frequent gekoloniseerd door bacteriën (Siddiqui, 2011; Hilt, 2014; Nicolle, 2019; Liedl, 2001). Bacteriurie kan vaak binnen 48 uur na plaatsing van een verblijfskatheter worden aangetoond, en de kans hierop stijgt met de duur dat de katheter langer blijft zitten tot uiteindelijk 100% (na een dag of zeven tot tien). Veelal betreft dit ‘kolonisatie’ van de katheter en urinewegen (asymptomatische bacteriurie), en geen infectie (zie ook module 1). De verwekkers van kathetergerelateerde urineweginfecties zijn voornamelijk darmbacteriën, die via de huid van het urogenitale gebied of de urethra de katheter koloniseren.
Het is niet aannemelijk dat het werken met een steriel veld en steriele handschoenen de kans op deze kolonisatie verkleint, mits de kathetertip lege artis steriel wordt gehouden (dat wil zeggen dat het deel dat in de patiënt achterblijft niet met de handen wordt aangeraakt). De werkgroep is daarom van mening dat werken met een schoon werkveld, en de reguliere handenhygiëne volstaat. Zie richtlijn Persoonlijke beschermingsmiddelen voor handschoengebruik.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Voor patiënten is het van belang dat een medische handeling veilig plaatsvindt. Elk risico dat zou kunnen bijdragen aan het ontstaan van een (zorggerelateerde) infectie zou moeten worden beperkt tot het minimum. Dit houdt in dat het de plicht is van de zorgmedewerker om handelingen zoals het inbrengen van een katheter op een zo veilig mogelijke manier uit te voeren. Hierbij is het van belang dat zorgmedewerkers die een katheter in brengen juist geschoold zijn en dat zij beschikken over de actuele protocollen met bijbehorende werkwijze.
Kosten (middelenbeslag)
Gemiddeld genomen zijn steriele, apart verpakte producten duurder dan een niet-steriele variant. Vanwege het feit dat deze vaker los verpakt zijn, en een extra verpakking hebben, kan dit ook meer transportkosten en kosten voor afvalverwerking opleveren. Daarnaast kost het meer tijd om steriel te werken, waardoor steriel werken meer personeelskosten met zich meebrengt. Aan de diagnostiek en behandeling van een urineweginfectie zijn ook kosten verbonden, dus bovenstaande besparingen zijn alleen terecht als dit niet leidt tot een toename van complicaties/infecties.
Aanvaardbaarheid, haalbaarheid en implementatie
Momenteel bestaat er veel praktijkvariatie in het schoon dan wel steriel werken rondom het inbrengen van een transurethrale katheter. Voor zorgmedewerkers die gewend zijn om steriel te werken, kan het onveilig voelen om het principe van steriel werken te verlaten. Hetzelfde geldt voor patiënten die gewend zijn dat hun katheter steriel wordt ingebracht. Juist omdat uit de literatuuranalyse blijkt dat er geen duidelijke meerwaarde bestaat van steriel werken in het voorkómen van (katheter gerelateerde) urineweginfecties, worden de voorwaarden voor een veilige katheter plaatsing laagdrempeliger. Mogelijk kost het minder tijd om schoon- dan steriel te werken, wat een tijdsbesparing oplevert voor zorgpersoneel. Ook is een mogelijk vervelende handeling voor de patiënt sneller voorbij.
Duurzaamheid
Steriele materialen zoals gaasjes en handschoenen bevatten vaak een extra verpakking, terwijl schone materialen samen in een grotere verpakking zitten. Ook moeten steriele materialen een extra bewerking ondergaan om steriel gemaakt te worden.
Daardoor geeft schoon werken ten opzichte van steriel werken een reductie van gebruik van CO2 en materialen, transportkosten en minder afval. Er loopt een onderzoek naar het gebruik van herbruikbare katheters. Totdat deze uitkomsten bekend zijn adviseert de werkgroep een steriele katheter te gebruiken.
Rationale van de aanbeveling
Op basis van de literatuur van (zeer) lage kwaliteit lijkt er geen duidelijke meerwaarde te bestaan van steriel ten opzichte van schoon werken ter voorkoming van een kathetergerelateerde urineweginfectie bij het plaatsen van een transurethrale katheter. De werkgroep is van mening dat schoon werken de nieuwe standaard is, omdat dit middelen, geld en tijd bespaart en duurzamer is. Daarnaast is er vanuit pathofysiologisch oogpunt weinig rationale voor steriel werken, zelfs bij een zichtbaar verontreinigde huid rondom de urethra.
Onderbouwing
Autorisatiedatum: 25 juni 2024
Eerstvolgende beoordeling actualiteit: 2026
Initiatief:
- Samenwerkingsverband Richtlijnen Infectiepreventie (SRI)
Geautoriseerd door:
- Nederlandse Vereniging van Internist-Infectiologen (NIV/NVII)
- Nederlandse Vereniging van Medische Microbiologie (NVMM)
- Nederlandse Vereniging voor Urologie (NVU)
- Nederlandse Vereniging voor Obstetrie en Gynaecologie (NVOG (Nederlandse Vereniging voor Obstetrie en Gynaecologie ))
- Nederlandse Orthopaedische Vereniging (NOV)
- Nederlandse Vereniging van Revalidatieartsen (VRA (Nederlandse Vereniging van Revalidatieartsen ))
- Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- Verpleegkundigen & Verzorgenden Nederland (V & VN)
- Patiëntenfederatie Nederland (PFNL (Patiëntfederatie Nederland ))
Regiehouder:
- SRI (Samenwerkingsverband Richtlijnen Infectiepreventie )
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd door het ministerie van VWS (Ministerie van Volksgezondheid, Welzijn en Sport). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
De huidige situatie voor infectiepreventiemaatregelen bij het inbrengen van een transurethrale katheter is niet eenduidig. Soms werkt men ‘schoon’ en soms werkt men ‘steriel’. Bij schoon werken wordt gebruik gemaakt van een onderlegger, worden niet-steriele handschoenen gedragen en worden de genitaliën gereinigd met leidingwater. Vervolgens wordt een steriele katheter ingebracht met de ‘no touch’-techniek.
Bij steriel werken wordt een steriel werkveld aangelegd, worden steriele handschoenen gebruikt, en worden de genitaliën gereinigd met steriel water. Steriel werken geeft meer kosten en lijkt minder duurzaam. Mocht dit onnodig blijken dan kan dit worden afgeschaft.
Deze module beschrijft de werkwijze voor het inbrengen van een transurethrale katheter.
A systematic review of the literature was performed to answer the following questions:
A. What is the effectiveness in preventing urinary tract infections of a clean technique for insertion of a transurethral catheter compared to a sterile technique?
P: Patient with/with an indication for a transurethral catheter.
I: Using a clean technique for insertion: non-sterile gloves, non-sterile field (disposable, non-sterile underpads), cleaning the genitals with tap water/water and soap / any other non-disinfectant.
C: Using a sterile technique for insertion: sterile gloves, sterile field (sterile underpad), cleaning the genitals with sterile water/disinfectant.
O: Urinary tract infection, bacteriuria.
B. What is the effectiveness in preventing urinary tract infections of cleaning the meatal area with water (tap water, water and soap, any other non-disinfectant) for insertion of a transurethral catheter compared to cleaning with sterile water or a disinfectant?
P: Patient with/with an indication for a transurethral catheter.
I: Cleaning the genitals with tap water/water and soap any other non-disinfectant.
C: Cleaning the genitals with sterile water/disinfectant.
O: Urinary tract infection, bacteriuria.
Relevant outcome measures
The guideline development group considered urinary tract infection as a critical outcome measure for decision making; and bacteriuria as an important outcome measure for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies. The working group defined the GRADE (Grading Recommendations Assessment, Development and Evaluation )-standard limit of 25% difference for dichotomous outcomes (RR < 0.8 or > 1.25), and 10% for continuous outcomes as a minimal clinically (patient) important difference.
Search and select (methods)
The databases Embase, Ovid/Medline and CINAHL were searched with relevant search terms from 2005 until 8th November 2022. The systematic literature search resulted in 748 hits. Studies were selected based on the following criteria: the study design was a systematic review or RCT, the study described a clean versus a sterile technique for insertion of a catheter or compared two or more cleaning methods for cleaning the genitals before catheter insertion, full text of the study was available, and full text was written in English or Dutch. Fifty-two studies were initially selected based on title and abstract screening. After reading the full text, 50 studies were excluded (see table of excluded studies), and one systematic review and one RCT were included.
Results
One systematic review and one RCTs were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables. The summary of literature, results and evidence tables are included in the appendix.
Description of studies
Mitchell (2021) conducted an updated systematic review on the effectiveness of antiseptic cleaning of the meatal area for the prevention of catheter-associated urinary tract infection (CAUTI) and bacteriuria in patients who receive a urinary catheter. The Cochrane Library, PubMed, Embase, The Cumulative Index to Nursing and Allied Health Literature (CINAHL), Medline and Academic Search Complete were searched from 1 January 2016 and 29 February 2020. Randomized controlled trials (RCTs) and quasi-experimental studies evaluating the use of antiseptic, antibacterial or non-medicated agents for cleaning the meatal, periurethral or perineal areas before indwelling catheter insertion or intermittent catheterisation or during routine meatal care. Data were extracted using the Cochrane Collaboration’s data collection form for RCTs and non-RCTs. One study (Duffy 1995; see below) compared a clean and a sterile technique for catheter insertion, and five studies compared clean and sterile methods for cleaning of the meatal area before catheter insertion. The term ‘infection’ was often referred to as the primary outcome in the studies included in the systematic review of Mitchell. However, the definition of infection varied and for most studies, this term was used when bacteria were present in the urine with or without clinical symptoms. Mitchell recoded outcomes to be either bacteriuria or infection—where the definition of infection must have included signs/symptoms of a urinary tract infection (UTI).
Duffy (1995) conducted an RCT to compare the safety of clean versus sterile intermittent bladder catheterisation in male nursing home residents. Eighty male residents of three long-term care facilities, ranging in age from 36 to 96 years with a mean age of 72 were included. Patients were randomized into clean and sterile IC (Intensive care) groups (n=42 in the sterile group, n=38 in the clean group). Standardized procedures for clean and sterile intermittent catheterisation (IC) were implemented by staff nurses at each site. The sterile procedure required all sterile equipment for each catheterisation, setting up of a sterile field with drapes, and cleansing of the urinary meatus with Betadine before catheterisation. Clean technique catheterisation does not require a sterile field and can be done in bed or chair as the patient desires. No cleaning of the meatus was done if normal daily hygiene (daily cleansing with soap and water) appeared sufficient and there was no obvious contamination with stool or other drainage. All catheterisation equipment was supplied by the pharmacy in a sterile condition. However, after the first use and for each catheterisation done during a one-week period, the catheter was simply washed with mild soap and running water, dried on a clean, lint free towel and stored at the patient’s bedside in a clean, dry container. Clean catheters were replaced each week. Average number of days in the study for the sterile groups was 63.6 and for the clean groups 63.8 days.
Khahakaew (2021) conducted an RCT to compare the efficacy of normal saline solution (NSS) and Savlon solution for periurethral cleaning in terms of catheter-associated bacteriuria and CAUTI prevention. A non-inferiority RCT was conducted with assignment to either NSS or Savlon (1.5% chlorhexidine gluconate combined with 15% cetrimide) periurethral cleaning solution before indwelling catheterisation. 10 mL of the Savlon solution was diluted into 1 L of sterile water (1:100 concentration), and the final solution used within 7 days. Each solution was randomly assigned to every participating hospital unit alternating every 3 months except the medical ICUs where NSS was used throughout the study period because the staff wished to continue their practice of not using Savlon. A urine culture was collected on day one (baseline urine culture), three and five of Foley catheter placement. If the patients had their catheter removed before day five it was assumed that the urine culture result on the remaining days would be the same. Patients admitted to a tertiary referral hospital from June 2018 to August 2019 participated in the study. The acceptable prespecified noninferiority margin was 10%. There were 265 and 275 patients in the NSS and Savlon groups, respectively.
Results
1. Urinary tract infection
A. Clean versus sterile technique for the insertion of a transurethral catheter
Duffy (1995) (described in Mitchell 2021) found that 21/38 patients (55%) in the ‘clean’ group developed a urinary tract infection compared to 26/42 patients (62%) in the ‘sterile’ group. The risk ratio was 0.89 (95% CI: 0.62 - 1.29). This is not a clinically relevant difference.
B. Clean versus sterile meatal area cleaning before insertion of a transurethral catheter
Two studies compared the effect of different cleaning methods of the meatal area on the outcome urinary tract infection. Fasugba (2019) (described in Mitchell 2021) compared cleaning the meatal area with normal saline compared to chlorhexidine. Thirteen patients (13/697) in the saline group developed a urinary tract infection compared to four (4/945) in the chlorhexidine group. The risk ratio was 4.41 (95% CI: 1.44 - 13.46). This is a clinically relevant difference.
Khahakaew (2021) compared normal saline solution with Savlon and found the incidence of CAUTI was 2.65/100 catheter-days for both groups total. The median duration of catheterisation was 5 (IQR 4,7) days. In the ‘normal saline solution’ group, the incidence was 0.355/100 catheter days in the Intention-to-treat analysis, in the Savlon group the incidence was 0.178/100 catheter days in the ITT analysis. The authors calculated an incidence rate ratio (IRR) of 2.07 (0.52–8.27) P=0.30 (ref=Savlon). This shows that there was no difference between the groups.
2. Bacteriuria
A. Clean versus sterile technique for the insertion of a transurethral catheter
None of the included studies described the outcome measure bacteriuria for the comparison clean versus sterile technique.
B. Clean versus sterile meatal area cleaning before insertion of a transurethral catheter
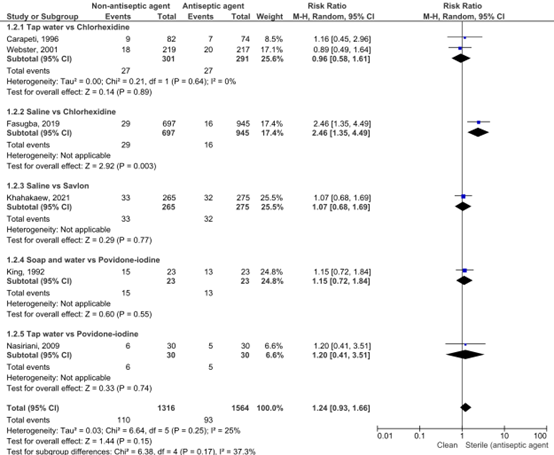
We calculated a pooled RR for the five studies included in Mitchell (2021) and the study of Khahakaew on the effect of using non-antiseptic meatal cleaning agent prior to catheter insertion, compared with an antiseptic agent, on the incidence of bacteriuria. The pooled RR was 1.24 [95% CI: 0.93 – 1.66] in favor of the use of antiseptics, with low heterogeneity (I2 = 25%). This is a not a clinically relevant difference.
Figure 2: Pooled RR Bacteriuria
Level of evidence of the literature
1. Urinary tract infection
A. Clean versus sterile technique for the insertion of a transurethral catheter
The level of evidence regarding the outcome measure UTI started at high and was downgraded by three levels to very low because of study limitations (-1; risk of bias: random sequence allocation and allocation concealment unclear, no blinding of participants and outcome assessors), and imprecision (-2; confidence interval overlaps both threshold for minimal clinically important difference).
B. Clean versus sterile meatal area cleaning before insertion of a transurethral catheter
The level of evidence regarding the outcome measure UTI started at high and was downgraded by three levels to very low because of study limitations (-1; risk of bias: allocation concealment and blinding unclear), inconsistency (-1; large difference between the effect of the included studies), imprecision (-1; confidence interval overlaps threshold for minimal clinically important difference).
2. Bacteriuria
A. Clean versus sterile technique for the insertion of a transurethral catheter
No evidence was found for a clean versus a sterile technique for the insertion of a transurethral catheter for the outcome measure bacteriuria.
B. Clean versus sterile meatal area cleaning before insertion of a transurethral catheter
The level of evidence regarding the outcome measure bacteriuria started at high and was downgraded by two levels to low because of study limitations (-1; risk of bias: allocation concealment and blinding unclear), and imprecision (-1; confidence interval overlaps minimal clinically important difference) to low.
1. Urinary tract infection
A. Clean versus sterile technique for the insertion of a transurethral catheter
|
Very low GRADE (Grading Recommendations Assessment, Development and Evaluation ) |
The evidence is very uncertain about the effect of a clean technique for the insertion of a transurethral catheter compared to a sterile technique for the outcome measure urinary tract infection. Source: Duffy (1995) from Mitchell (2021) |
|---|
B. Clean versus sterile meatal area cleaning before insertion of a transurethral catheter
|
Very low GRADE |
The evidence is very uncertain about the effect of a non-antiseptic meatal cleaning agent on urinary tract infection when compared with an antiseptic meatal cleaning agent. Source: Mitchell (2021), Khahakaew (2021) |
|---|
2. Bacteriuria
A. Clean versus sterile technique for the insertion of a transurethral catheter
|
No GRADE |
No evidence was found on the effect of a clean technique for the insertion of a transurethral catheter compared to a sterile technique for the outcome measure bacteriuria. Source: - |
|---|
B. Clean versus sterile meatal area cleaning before insertion of a transurethral catheter
|
Low GRADE |
Using a non-antiseptic meatal cleaning agent prior to catheter insertion may result in little to no difference in bacteriuria when compared with an antiseptic agent. Source: Mitchell (2021), Khahakaew (2021) |
|---|
Duffy LM, Cleary J, Ahern S, Kuskowski MA, West M, Wheeler L, Mortimer JA. Clean intermittent catheterization: safe, cost-effective bladder management for male residents of VA nursing homes. J Am Geriatr Soc. 1995 Aug;43(8):865-70. doi: 10.1111/j.1532-5415.1995.tb05528.x. PMID: 7636093.
Hilt EE, McKinley K, Pearce MM, Rosenfeld AB, Zilliox MJ, Mueller ER, Brubaker L, Gai X, Wolfe AJ, Schreckenberger PC. Urine is not sterile: use of enhanced urine culture techniques to detect resident bacterial flora in the adult female bladder. J Clin Microbiol. 2014 Mar;52(3):871-6. Doi: 10.1128/JCM.02876-13. Epub 2013 Dec 26. PMID: 24371246; PMCID: PMC3957746.
Khahakaew S, Suwanpimolkul G, Wongkeskij T, Punakabutra N, Suankratay C. A comparison of the efficacy of normal saline and Savlon solutions in periurethral cleaning to reduce catheter-associated bacteriuria: A randomized control trial. Int J Infect Dis. 2021 Apr;105:702-708. doi: 10.1016/j.ijid.2021.02.086. Epub 2021 Feb 23. PMID: 33636356.
Liedl B. Catheter-associated urinary tract infections. Curr Opin Urol. 2001 Jan;11(1):75-9. doi: 10.1097/00042307-200101000-00011. PMID: 11148750.
Mitchell B, Curryer C, Holliday E, Rickard CM, Fasugba O. Effectiveness of meatal cleaning in the prevention of catheter-associated urinary tract infections and bacteriuria: an updated systematic review and meta-analysis. BMJ Open. 2021 Jun 8;11(6):e046817. doi: 10.1136/bmjopen-2020-046817. PMID: 34103320; PMCID: PMC8190044.
Nicolle LE, Gupta K, Bradley SF, Colgan R, DeMuri GP, Drekonja D, Eckert LO, Geerlings SE, Köves B, Hooton TM, Juthani-Mehta M, Knight SL, Saint S, Schaeffer AJ, Trautner B, Wullt B, Siemieniuk R. Clinical Practice Guideline for the Management of Asymptomatic Bacteriuria: 2019 Update by the Infectious Diseases Society of America. Clin Infect Dis. 2019 May 2;68(10):1611-1615. doi: 10.1093/cid/ciz021. PMID: 31506700.
Siddiqui H, Nederbragt AJ, Lagesen K, Jeansson SL, Jakobsen KS. Assessing diversity of the female urine microbiota by high throughput sequencing of 16S rDNA amplicons. BMC Microbiol. 2011 Nov 2;11:244. doi: 10.1186/1471-2180-11-244. PMID: 22047020; PMCID: PMC3228714.
Bekijk de Evidence-tabel:
|
Reference |
Reason for exclusion |
|---|---|
|
Al-Farsi, S. and Oliva, M. and Davidson, R. and Richardson, S. E. and Ratnapalan, S. Periurethral cleaning prior to urinary catheterization in children: Sterile water versus 10% povidone-iodine. Clinical Pediatrics. 2009; 48 (6) :656-660. |
Wrong P (Patients received a catheter because of suspected UTI) |
|
Fasugba, O. and Koerner, J. and Mitchell, B. G. and Gardner, A. Systematic review and meta-analysis of the effectiveness of antiseptic agents for meatal cleaning in the prevention of catheter-associated urinary tract infections. Journal of Hospital Infection. 2017; 95 (3) :233-242. |
Updated by Mitchell 2021 |
|
Ercole, F. F. and Macieira, T. G. R. and Wenceslau, L. C. C. and Martins, A. R. and Campos, C. C. and Chianca, T. C. M. Integrative review: Evidences on the practice of intermittent/indwelling urinary catheterization. Revista Latino-Americana de Enfermagem. 2013; 21 (1) :459-468. |
Not a systematic review (integrative review) |
|
Cunha, M. and Santos, E. and Andrade, A. and Jesus, R. and Aguiar, C. and Marques, F. and Enes, F. and Santos, M. and Fernandes, R. and Soares, S. [Effectiveness of cleaning or disinfecting the urinary meatus before urinary catheterization: a systematic review]. Revista da Escola de Enfermagem da U S P. 2013; 47 (6) :1410-1416. |
Poor Quality, no search date available, old SR, studies also included in Huang |
|
Mitchell, B. G. and Fasugba, O. and Cheng, A. C. and Gregory, V. and Koerner, J. and Collignon, P. and Gardner, A. and Graves, N. Chlorhexidine versus saline in reducing the risk of catheter associated urinary tract infection: A cost-effectiveness analysis. International journal of nursing studies. 2019; 97 :1-6. |
Cost-effectiveness study |
|
Mitchell, Brett G. Meatal cleansing with chlorhexidine reduces catheter-associated infection. Nursing Times. 2019; 115 (9) :21-22. |
No research paper, repetition of data published elsewhere |
|
Fasugba, O. and Cheng, A. C. and Gregory, V. and Graves, N. and Koerner, J. and Collignon, P. and Gardner, A. and Mitchell, B. G. Chlorhexidine for meatal cleaning in reducing catheter-associated urinary tract infections: a multicentre stepped-wedge randomised controlled trial. The Lancet Infectious Diseases. 2019; 19 (6) :611-619. |
Is included in the SR or Mitchell 2021 |
|
Yan, Liu and Dong, Xiao and Xiao-hui, Shi and Liu, Yan and Xiao, Dong and Shi, Xiao-Hui Urinary tract infection control in intensive care patients. Medicine. 2018; 97 (38) :1-3. |
Not an RCT |
|
Nugraha, A. and Puspita, T. and Patimah, I. I. N. and Nagara, A. D. Comparison of 10% povidone iodine and sterile water as a periuretra cleansing solution before the insertion of indwelling urine cathether on the occurance of bacteria. International Journal of Pharmaceutical Research. 2019; 11 (4) :810-816. |
Not an RCT |
|
Araujo da Silva, A. R. and Marques, A. F. and Biscaia di Biase, C. and Zingg, W. and Dramowski, A. and Sharland, M. Interventions to prevent urinary catheter–associated infections in children and neonates: a systematic review. Journal of Pediatric Urology. 2018; 14 (6) :556.e1-556.e9. |
No systematic summary of results, all study designs included (often no control group in included studie) |
|
Sreeramoju, P. Preventing healthcare-associated infections: Beyond best practice. American Journal of the Medical Sciences. 2013; 345 (3) :239-244. |
Not a SR or RCT |
|
Flagg, Laura R. and Julien, David Martin and Lajiness, Michelle J. and Thompson, Donna L. Urinary Catheterization of the Adult Male. Urologic Nursing. 2021; 41 (2) :70-75. |
Not a SR or RCT |
|
Ramezani, F. and Khatiban, M. and Rahimbashar, F. and Soltanian, A. R. Efficacy of bladder irrigation in preventing urinary tract infections associated with short-term catheterization in comatose patients: A randomized controlled clinical trial. American Journal of Infection Control. 2018; 46 (10) :e45-e50. |
Bladder irrigation |
|
Diniz, Iraktania Vitorino and Guimaraes Oliveira Soares, Maria Júlia Clinical-epidemiological profile and clean intermittent catheterization in people with spinal cord injury. Online Brazilian Journal of Nursing. 2017; 16 :6-6. |
Not an original study or SR, description of epidemiological profile |
|
Panchisin, Teresa EB93 Use of Castile Soap for Indwelling Urinary Catheter Care in Critically Ill Patients. Critical Care Nurse. 2014; 34 (2) :e24-e24. |
Conference abstract |
|
Levers, Helen Switching to an antimicrobial solution for skin cleansing before urinary catheterisation. British Journal of Community Nursing. 2014; 19 (2) :66-71. |
Not a SR or RCT, description of policy change |
|
He W, Wang D, Ye Z, Qian W, Tao Y, Shi X, Liu L, Chen J, Qiu L, Wan P, Jia X, Li X, Gao C, Ma X, Wen B, Chen N, Li P, Ren Z, Lan L, Li S, Zuo Y, Zhang H, Ma L, Zhang Y, Li Z, Su W, Yang Q, Chen Q, Wang X, Ye Z, Chen JP, Loo WT, Chow LW, Yip AY, Ng EL, Cheung MN, Wang Z. Application of a nanotechnology antimicrobial spray to prevent lower urinary tract infection: a multicenter urology trial. J Transl Med. 2012 Sep 19;10 Suppl 1(Suppl 1):S14. doi: 10.1186/1479-5876-10-S1-S14. Epub 2012 Sep 19. PMID: 23046566; PMCID: PMC3445864. |
Combination of insertion and daily care |
|
Choi, J. S. and Yeon, J. H. Effects of perineal care in preventing catheter associated urinary tract infections (CAUTI) in intensive care units (ICU). Journal of Korean Academy of Fundamentals of Nursing. 2012; 19 (2) :1p-1p. |
Article in Korean language |
|
Peng X, Qian W, Zhuang J, Zhang J, Wang Z, Shen L, Chang Q, Gu X, Shi J, Hou J. Optimizing the Catheter Care and Maintenance Strategy of Short-Term Catheterization among Hospitalized Patients in Microbiological Approach. Biomed Res Int. 2020 Nov 28;2020:1971324. doi: 10.1155/2020/1971324. Retraction in: Biomed Res Int. 2024 Mar 20;2024:9786204. doi: 10.1155/2024/9786204. PMID: 33313311; PMCID: PMC7719536. |
Wrong I/Wrong C |
|
Sweeney, A. Suprapubic Catheter Change Methods: A Crossover Comparison Cohort Trial. Journal of wound, ostomy, and continence nursing : official publication of The Wound, Ostomy and Continence Nurses Society. 2017; 44 (4) :368-373. |
Wrong P (suprapubische katheter) |
|
Araujo da Silva, A. R. and Marques, A. F. and Biscaia di Biase, C. and Zingg, W. and Dramowski, A. and Sharland, M. Interventions to prevent urinary catheter-associated infections in children and neonates: a systematic review. Journal of pediatric urology. 2018; 14 (6) :556.e1-556.e9. |
Double |
|
Bermingham, Sarah L. and Hodgkinson, Sarah and Wright, Sue and Hayter, Ellie and Spinks, Julian and Pellowe, Carol Intermittent self catheterisation with hydrophilic, gel reservoir, and non-coated catheters: a systematic review and cost effectiveness analysis. BMJ (Clinical research ed.). 2013; 346 :e8639. |
Wrong I/C (study on the material of the catheter) |
|
Sinclair, L. and Hagen, S. and Cross, S. Washout policies in long-term indwelling urinary catheterization in adults: A short version cochrane review. Neurourology and Urodynamics. 2011; 30 (7) :1208-1212. |
Wrong I (I to prevent catheter blockage) |
|
Moola, Sandeep and Konno, Rie A systematic review of the management of short-term indwelling urethral catheters to prevent urinary tract infections. JBI library of systematic reviews. 2010; 8 (17) :695-729. |
More recent SR available (Mitchell 2021) |
|
Hung, Allie and Giesbrecht, Natasha and Pelingon, Poli and Bissonnette, Rebecca Sterile water versus antiseptic agents as a cleansing agent during periurethral catheterizations. NEOutlook. 2010; 33 (2) :18-21. |
Low quality review |
|
Hagen, S. and Sinclair, L. and Cross, S. Washout policies in long-term indwelling urinary catheterisation in adults. Cochrane database of systematic reviews (Online). 2010; 3: CD004012. |
Wrong I (to prevent catheter blockage) |
|
Willson, M. and Wilde, M. and Webb, M. L. and Thompson, D. and Parker, D. and Harwood, J. and Callan, L. and Gray, M. Nursing interventions to reduce the risk of catheter-associated urinary tract infection: part 2: staff education, monitoring, and care techniques. Journal of wound, ostomy, and continence nursing: official publication of The Wound, Ostomy and Continence Nurses Society / WOCN. 2009; 36 (2) :137-154. |
Review but not SR |
|
Medical Advisory, Secretariat Hydrophilic catheters: an evidence-based analysis. Ontario health technology assessment series. 2006; 6 (9) :1-31. |
Wrong I/C (study on the material of the catheter) |
|
Sönmez Duzkaya, Düygu and Uysal, Gülzade and Bozkurt, Gülçin and Yakut, Tülay and Çitak, Agop Povidone-Iodine, 0.05% Chlorhexidine Gluconate, or Water for Periurethral Cleaning Before Indwelling Urinary Catheterization in a Pediatric Intensive Care. Journal of Wound, Ostomy & Continence Nursing. 2017; 44 (1) :84-88. |
Double |
|
Samimi, Gh and Ezzati, Zh and Sarokhani, M. R. and Mosalii, S. S. and Mehrabi, Y. Effects of bladder irrigation with chlorhexidine and normal saline on prevention of bacteriuria in patient with foley catheter. Advances in Nursing & Midwifery. 2010; 20 (70) :57-57. |
Wrong I/C (bladder irrigation) |
|
Sublett, C. M. Translating evidence into clinical practice. Adding to the evidence base: comparison of the effect of water vs. povidone-iodine solution for periurethral cleaning in women requiring an indwelling catheter prior to gynecologic surgery. Urologic Nursing. 2009; 29 (2) :122-123. |
Methodological paper on Phase III trials and their application in practice |
|
Pellowe, C. Practice question: solving your clinical dilemmas. Nursing Times. 2009; 105 (26) :19-19. |
Not a research paper (Practice question) |
|
Nasiriani, K. and Kalani, Z. and Farnia, F. and Motavasslian, M. and Nasiriani, F. and Engberg, S. Comparison of the effect of water vs. povidone-iodine solution for periurethral cleaning in women requiring an indwelling catheter prior to gynecologic surgery. Urologic nursing: official journal of the American Urological Association Allied. 2009; 29 (2) :118-121, 131. |
Included in Mitchell 2021 |
|
Moore, K. N. and Hunter, K. F. and McGinnis, R. and Bacsu, C. and Fader, M. and Gray, M. and Getliffe, K. and Chobanuk, J. and Puttagunta, L. and Voaklander, D. C. Do catheter washouts extend patency time in long-term indwelling urethral catheters? A randomized controlled trial of acidic washout solution, normal saline washout, or standard care. Journal of wound, ostomy, and continence nursing: official publication of The Wound, Ostomy and Continence Nurses Society / WOCN. 2009; 36 (1) :82-90. |
Wrong I (catheter washout) |
|
Jeong, I. and Park, S. and Jeong, J. S. and Kim, D. S. and Choi, Y. S. and Lee, Y. S. and Park, Y. M. Comparison of catheter-associated urinary tract infection rates by perineal care agents in intensive care units. Asian Nursing Research. 2010; 4 (3) :142-150. |
Included in Mitchell 2020 |
|
Percival, S. L. and Sabbuba, N. A. and Kite, P. and Stickler, D. J. The effect of EDTA instillations on the rate of development of encrustation and biofilms in Foley catheters. Urological Research. 2009; 37 (4) :205-209 |
Wrong I/C |
|
Williams, G. J. and Stickler, D. J. Some observations on the diffusion of antimicrobial agents through the retention balloons of foley catheters. The Journal of urology. 2007; 178 (2) :697-701. |
Wrong I/C |
|
Sekiguchi, Y. and Yao, Y. and Ohko, Y. and Tanaka, K. and Ishido, T. and Fujishima, A. and Kubota, Y. Self-sterilizing catheters with titanium dioxide photocatalyst thin films for clean intermittent catheterization: Basis and study of clinical use. International Journal of Urology. 2007; 14 (5) :426-430. |
Does not meet PICO (material of catheter) |
|
Fasugba, Oyebola and Koerner, Jane and Mitchell, Brett G. and Gardner, Anne Meatal cleaning with antiseptics for the prevention of catheter-associated urinary tract infections: A discussion paper. Infection, disease & health. 2017; 22 (3) :136-143. |
Wrong design (discussion paper) |
|
Cooper. Policies for replacing long-term indwelling urinary catheters in adults. 2016. |
More recent SR available (Mitchell 2021) |
|
Kiddoo, D. and Sawatzky, B. and Bascu, C. D. and Dharamsi, N. and Afshar, K. and Moore, K. N. Randomized Crossover Trial of Single Use Hydrophilic Coated vs Multiple Use Polyvinylchloride Catheters for Intermittent Catheterization to Determine Incidence of Urinary Infection. The Journal of urology. 2015; 194 (1) :174-179. |
Wrong I/C (material of catheter) |
|
Bermingham SL, Hodgkinson S, Wright S, Hayter E, Spinks J, Pellowe C. Intermittent self catheterisation with hydrophilic, gel reservoir, and non-coated catheters: a systematic review and cost effectiveness analysis. BMJ. 2013 Jan 8;346:e8639. doi: 10.1136/bmj.e8639. PMID: 23303886; PMCID: PMC3541473. |
Wrong I/C (compares different materials of catheters) |
|
Zakaria, Nordin and Nasir, Ariffin and Van Rostenberghe, Hans and Ilias, Mohamad Ikram Sterile Water Versus Chlorhexidine as Cleaning Agent for Clean Intermittent Catheterization in Children: A Randomized Controlled Trial. International Medical Journal. 2020; 27 (6) :666-669. |
Wrong P (children with a neurgenic bladder) |
|
Sarani, Hamed and Mofrad, Zahra Pishkar and Faghihi, Hamed and Ghabimi, Mehrangiz Comparison of the Effect of Perineal Care with Normal Saline and 2% Chlorhexidine Solution on the Rate of Catheter-Associated Urinary Tract Infection inWomen Hospitalized in Intensive Care Units: A Quasi-Experimental Study. Medical-Surgical Nursing Journal. 2020; 9 (2) :1-8. |
Describes daily care (not catheter insertion) |
|
Peter, S. and Devi, E. S. and Nayak, S. G. Effectiveness of clinical practice guidelines on prevention of catheter-associated urinary tract infections in selected hospitals. Journal of Krishna Institute of Medical Sciences University. 2018; 7 (1) :55-66. |
Wrong design (No SR or RCT), evaluates implementation of policy |
|
Wilson, Mary Addressing the problems of long-term urethral catheterization: part 1. British Journal of Nursing. 2011; 20 (22) :1418-1424. |
Narrative review |
|
Cheung, K. and Leung, P. and Wong, Y. c and To, O. k and Yeung, Y. f and Chan, M. w and Yip, Y. l and Kwok, C. w Water versus antiseptic periurethral cleansing before catheterization among home care patients: A randomized controlled trial. American Journal of Infection Control. 2008; 36 (5) :375-380 |
Very low number of participants |
|
Huang, K. and Liang, J. and Mo, T. and Zhou, Y. and Ying, Y. Does periurethral cleaning with water prior to indwelling urinary catheterization increase the risk of urinary tract infections? A systematic review and meta-analysis. American Journal of Infection Control. 2018; 46 (12) :1400-1405. |
More recent SR available (Mitchell 2021) |
|
Sönmez Düzkaya, Duygu and Uysal, Gülzade and Yakut, Tülay and Çıtak, Agop A RANDOMIZED CONTROLLED TRIAL: POVIDONE IODINE, CHLORHEXIDINE OR WATER FOR PERIURETHRAL CLEANING BEFORE URINARY CATHETERIZATION IN PEDIATRIC INTENSIVE CARE. CONNECT: The World of Critical Care Nursing. 2014; 9 (3) :64-64. |
Conference abstract |
|
Düzkaya DS, Uysal G, Bozkurt G, Yakut T, Çitak A. Povidone-Iodine, 0.05% Chlorhexidine Gluconate, or Water for Periurethral Cleaning Before Indwelling Urinary Catheterization in a Pediatric Intensive Care: A Randomized Controlled Trial. J Wound Ostomy Continence Nurs. 2017 Jan/Feb;44(1):84-88. doi: 10.1097/WON.0000000000000280. PMID: 27824737. |
Wrong I/C (compares different antiseptics) |
Bekijk de Risk-of-bias-tabel:
Bijlagen
| Begrip | Definitie |
|---|---|
|
UWI |
Urinary tract infection/urineweginfectie. |
|
CAUTI |
Catheter-associated urinary tract infection/kathetergerelateerde urineweginfectie. |
|
Algemene voorzorgsmaatregelen |
Maatregelen die bij elke patiënt ongeacht zijn/haar infectiestatus of kolonisatie van toepassing zijn. Deze maatregelen staan beschreven in de SRI (Samenwerkingsverband Richtlijnen Infectiepreventie )-richtlijnen Handhygiëne & persoonlijke hygiëne medewerker, Persoonlijke beschermingsmiddelen, Reiniging & desinfectie van ruimten en Accidenteel bloedcontact. |
|
Antibioticaprofylaxe |
Een antibioticumgift ter voorkoming van een infectie bij een ingreep of instrumentatie van de urinewegen, in principe eenmalig. |
|
Bacteriurie |
Aantoonbare bacteriën in de urine zonder klachten. |
|
Blaaskatheter |
En slangetje dat via de urethra (transurethrale katheter) of via de buik (suprapubische katheter) in de blaas wordt gebracht en de urine afvoert. |
|
Urineweginfectie |
Door micro-organismen geïnduceerde ontstekingsreactie van nier, pyelum, ureter, blaas, urethra, prostaat, testes en/of epididymis. |
|
Suprapubische katheter |
Een suprapubische katheter is een katheter die via de buik, boven het schaambeen langs, in de blaas wordt gebracht. |
|
Transurethrale katheter |
Een slangetje dat voor langere tijd via de urethra (plasbuis) in de blaas wordt gebracht om urine uit uw blaas te laten lopen. |
|
Intermitterend katheteriseren |
Intermitterend katheteriseren is het herhaaldelijk, met tussenpozen, legen van de blaas met een eenmalige katheter die wordt ingebracht via de urinebuis. |
|
Urineopvangzak |
Een urineopvangzak wordt gebruikt om de urine uit de blaas op te vangen wanneer een katheter is ingebracht. |
|
Nachtzak |
Een urineopvangzak met grote inhoud die aan het bed van de patiënt bevestigd wordt. |
|
Beenzak |
Een beenzak/dagzak is een urineopvangzak die met banden of een fixatiekous aan het been wordt bevestigd. |
|
Dagzak |
Zie beenzak. |
Werkwijze
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met een blaaskatheter. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere WIP-richtlijn Blaaskatheterisatie op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door NOV (Nederlandse Orthopaedische Vereniging ), NVZ, Verenso (Vereniging van specialisten ouderengeneeskunde ), VHIG (Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg ), PFNL (Patiëntfederatie Nederland ), NVMM (Nederlandse Vereniging voor Medische Microbiologie ), NVOG (Nederlandse Vereniging voor Obstetrie en Gynaecologie ), NVU, VRA (Nederlandse Vereniging van Revalidatieartsen ), VCCN via een schriftelijke knelpunteninventarisatie. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Ook definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie www.gradeworkinggroup.org). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|---|---|
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID (Minimal Clinically Important Difference )). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|---|---|---|
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van de Patiëntenfederatie Nederland (PFNL) voor de knelpunteninventarisatie. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan PFNL en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz (Wet kwaliteit, klachten en geschillen zorg ) & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst raming |
Toelichting |
|---|---|---|
|
Indicaties |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het overgrote deel (± 90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen financiële gevolgen verwacht. |
|
Inbrengen |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Dagelijkse verzorging |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het overgrote deel (± 90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen financiële gevolgen verwacht |
|
Katheterwissel |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R,Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S,Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in healthcare. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group,2013.
Dit implementatieplan is opgesteld om de implementatie van de aanbevelingen in de richtlijn infectiepreventie Blaaskatheterisatie te borgen. Voor het opstellen van dit plan heeft de werkgroep per ontwikkelde module beoordeeld wat eventueel bevorderende en belemmerende factoren zijn voor het naleven van de aanbevelingen en wat eventueel nodig is om de aanbevolen infectiepreventiemaatregelen in Nederland te implementeren.
Werkwijze
De werkgroep heeft per aanbeveling binnen de modules geïnventariseerd:
- wat een realistische termijn voor implementatie is;
- de verwachtte effect van implementatie op de zorgkosten;
- randvoorwaarden om de aanbeveling tijdig te implementeren;
- mogelijk barrières voor implementatie;
- te ondernemen acties voor (bevordering van) implementatie;
- verantwoordelijke partij voor de te ondernemen acties.
Hieronder is een tabel (tabel 1) opgenomen met alle modules uit deze richtlijn met daarbij de bijhorende implementatietermijn, verwacht effect op kosten, mogelijke barrières voor implementatie, te ondernemen acties voor implementatie en verantwoordelijken voor de acties.
Tabel 1 Implementatieplan
|
Module |
Tijdspad voor implementatie |
Verwacht effect op de kosten |
Mogelijke barrières voor implementatie |
Te ondernemen acties voor implementatie |
Verantwoordelijke voor acties
|
|---|---|---|---|---|---|
|
Indicaties |
<1 jaar |
Geen, betreft grotendeels bestaand beleid |
Geen |
Verspreiden richtlijn en voorlichten zorgmedewerkers |
Professionals |
|
Inbrengen |
<1 jaar |
Kostenreductie doordat beleid is aangepast naar schoon inbrengen i.p.v. steriel |
Weerstand tegen verandering van zorgverleners die gewend zijn om steriel te werken |
Verspreiden richtlijn en voorlichten zorgmedewerkers |
Professionals |
|
Dagelijkse verzorging |
<1 jaar |
Geen, dit betreft grotendeels bestaand beleid |
Geen |
Verspreiden richtlijn en voorlichten zorgmedewerkers |
Professionals |
|
Katheterwissel |
<1 jaar |
Geen, dit betreft grotendeels bestaand beleid |
Geen |
Verspreiden richtlijn en voorlichten zorgmedewerkers |
Professionals |
Termijn voor implementatie
Omdat de aanbevelingen in het algemeen nauw aansluiten bij de huidige klinische praktijk, voorziet de werkgroep nauwelijks belemmeringen voor implementatie. Als men ervan uitgaat dat alle betrokken zorgprofessionals vanaf autorisatie van deze richtlijn (voorzien begin 2024) binnen een jaar op de hoogte gesteld worden van deze richtlijn, is implementatie van de aanbevelingen vanaf een jaar later (begin 2025) realistisch en haalbaar.
Te ondernemen acties per partij
Hieronder wordt per partij toegelicht welke acties zij kunnen ondernemen om de implementatie van de richtlijn te bevorderen.
Alle direct betrokken wetenschappelijke verenigingen/beroepsorganisaties
- Bekend maken van de richtlijn onder de leden.
- Publiciteit voor de richtlijn door er over te vertellen op congressen.
- Ontwikkelen van gerichte bijscholing/trainingen om kennisoverdracht tussen medewerkers te faciliteren/stimuleren.
- Ontwikkelen en aanpassen van infectiepreventieprotocollen.
De lokale vakgroepen/individuele medisch professionals
- Het bespreken van de aanbevelingen in de multidisciplinaire teamoverleggen, vakgroepoverleggen en relevante lokale werkgroepen.
- Aanpassen lokale infectiepreventieprotocollen.
- Afstemmen en afspraken maken met andere betrokken disciplines om de toepassing van de aanbevelingen in de praktijk te borgen.
Samenwerkingsverband Richtlijnen Infectiepreventie (SRI):
- Toevoegen van de richtlijn aan de SRI (Samenwerkingsverband Richtlijnen Infectiepreventie )-website.
- Toevoegen van richtlijn aan richtlijnendatabase.
- Het implementatieplan wordt in de bijlage opgenomen, zodat deze voor op een voor alle partijen goed te vinden is.
- De kennislacunes worden opgenomen in de bijlagen.
Indicatoren
Voor deze richtlijn zijn geen indicatoren ontwikkeld.
Tijdens de ontwikkeling van de richtlijn Blaaskatheterisatie is systematisch gezocht naar onderzoeksbevindingen die nuttig konden zijn voor het beantwoorden van de uitgangsvragen. Een deel (of een onderdeel) van de hiervoor opgestelde zoekvragen is met het resultaat van deze zoekacties te beantwoorden, een deel echter niet. Door gebruik te maken van de evidence-based methodiek (EBRO) is duidelijk geworden dat er nog kennislacunes bestaan. De werkgroep is van mening dat (vervolg)onderzoek wenselijk is om in de toekomst een duidelijker antwoord te kunnen geven op vragen uit de praktijk. Om deze reden heeft de werkgroep per module aangegeven waar wetenschappelijke kennis beperkt is en dus op welke vlakken nader onderzoek gewenst is.
Module 1 Indicaties
Wat is het effect van intermitterend katheteriseren op het ontstaan van een urineweginfectie en bacteriurie in vergelijking met een verblijfskatheter?
Wat is het effect van een suprapubische katheter op het ontstaan van een urineweginfectie en bacteriurie in vergelijking met een verblijfskatheter?
Zijn er verschillende uitkomsten voor verschillende patiëntengroepen bij de twee bovenstaande vragen (bijvoorbeeld patiënten met neurogene blaas na operatie of oudere patiënten)?
Module 2 Inbrengen
Bij module 2 zijn geen kennislacunes geformuleerd.
Module 3 Dagelijkse verzorging
- Wat is het effect van hergebruik van een urine(nacht)zak ten opzichte van eenmalig gebruik van een urine(nacht)zak bij patiënten met een transurethrale katheter op het ontstaan van een urineweginfectie of bacteriurie?
- Wat is het effect van het aansluiten van een katheterzak met een hoog volume (nachtzak) op de afvoerklep van een katheterbeenzak in vergelijking met het verwisselen van de dag- en nacht-urinezak voor de nacht bij patiënten met een transurethrale katheter op het optreden van een urineweginfectie of bacteriurie?
Module 4 Katheterwissel
De werkgroep ziet het ontbreken van bewijs voor een wisselstrategie van een urinekatheter in het voorkomen van infecties bij patiënten met en zonder risicofactoren als kennislacune. Studies naar een vergelijking van een vastgesteld wisselmoment op vier weken versus zes weken versus twaalf weken zouden kunnen voorzien in bewijsvoering.
Bekijk de pdf met de notulen van de schriftelijke knelpunteninventarisatie voor deze richtlijn.